Jelita jako strażnik układu odpornościowego? Co faktycznie wynika z badań
Związek między jelitami a układem odpornościowym jest tematem, który coraz częściej pojawia się w literaturze naukowej i medycznych dyskusjach klinicznych. Trudno się temu dziwić — przewód pokarmowy jest miejscem, w którym organizm ma największy kontakt ze środowiskiem zewnętrznym, a jednocześnie jednym z najważniejszych obszarów aktywności immunologicznej. Warto jednak trzymać się faktów i wyjaśnić, jak wygląda to w świetle aktualnej wiedzy.
Dlaczego jelita odgrywają tak istotną rolę w odporności?
Śluzówka jelit to powierzchnia rzędu 30–40 m², co czyni ją największym interfejsem między organizmem a otoczeniem. Z tego powodu skoncentrowana jest tam rozbudowana sieć tkanek limfatycznych — GALT (Gut-Associated Lymphoid Tissue).
W publikacjach naukowych podkreśla się, że znacząca część komórek odpornościowych organizmu rezyduje właśnie w obrębie GALT. Często cytowana liczba 70–80% jest uproszczeniem wynikającym z różnych metod liczenia, ale sam fakt dominującej roli jelit jest dobrze udokumentowany: immunologia jelit to fundamentalny element odporności.
GALT jako system rozpoznawania bodźców
GALT pełni funkcję biologicznego „punktu decyzyjnego”, w którym układ immunologiczny ocenia:
- składniki pokarmowe,
- mikrobiotę fizjologiczną,
- bakterie patogenne,
- toksyny i substancje drażniące.
W prawidłowych warunkach mechanizmy tolerancji — zależne m.in. od komórek dendrytycznych, limfocytów T regulatorowych i cytokin przeciwzapalnych — umożliwiają spokojną reakcję na pożywienie i mikrobiotę. Reakcja zapalna uruchamiana jest dopiero w sytuacji realnego zagrożenia.
Bariery jelitowe a autoimmunologia
Jednym z najlepiej przebadanych aspektów immunologii jelit jest związek między zwiększoną przepuszczalnością bariery jelitowej a ryzykiem przewlekłej aktywacji układu odpornościowego. Mechanizm ten opisano m.in. w kontekście:
- celiakii (z rolą zonuliny potwierdzoną mechanistycznie),
- nieswoistych zapaleń jelit (IBD),
- cukrzycy typu 1,
- niektórych chorób tarczycy (dowody głównie obserwacyjne).
Wbrew prostym narracjom, nie oznacza to, że choroby autoimmunologiczne zaczynają się w jelitach. Obowiązujący model jest wieloczynnikowy: do rozwoju autoagresji przyczynia się kombinacja predyspozycji genetycznych, czynników środowiskowych, infekcji, procesów hormonalnych i zaburzeń regulacji immunologicznej. Jelita są jednym z elementów, ale nie jedynym „winowajcą”.
Czy poprawa funkcji jelit wpływa na przebieg autoagresji?
Interwencje żywieniowe i modyfikacja mikrobioty mogą wpływać na intensywność reakcji zapalnych. W badaniach klinicznych obserwuje się:
- zmniejszenie markerów zapalnych,
- poprawę funkcji bariery jelitowej,
- redukcję objawów u części pacjentów.
Nie stanowią jednak samodzielnego leczenia autoimmunologii. Mogą być natomiast wartościowym elementem terapii wspomagającej — pod warunkiem, że są prowadzone równolegle z leczeniem specjalistycznym.
Podsumowanie
Jelita odgrywają ważną rolę w regulacji odporności dzięki rozbudowanej tkance GALT oraz interakcji z mikrobiotą. Zaburzenia tej równowagi mogą sprzyjać nadmiernej aktywacji immunologicznej, co w określonych sytuacjach ma znaczenie dla przebiegu chorób autoimmunologicznych. Jednocześnie obecny stan wiedzy nie wspiera redukcjonistycznych teorii, według których autoagresja wynika wyłącznie z „nieszczelnych jelit”. To raczej jeden z wielu czynników wpływających na złożoną sieć procesów immunologicznych.
Zobacz również

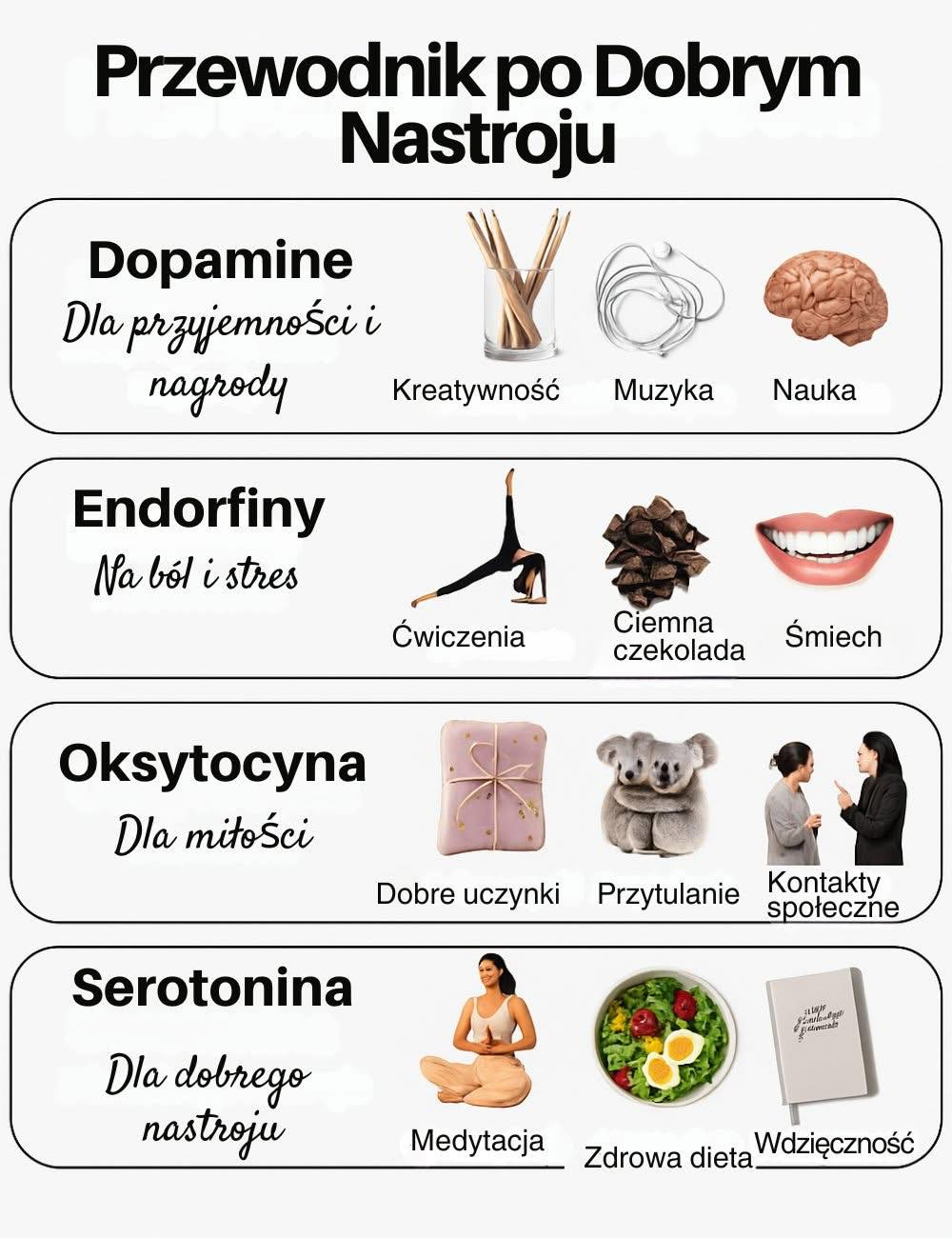
Szczęśliwe hormony – jak je aktywować?
10 lutego 2024
Rodzina to twój największy skarb
19 stycznia 2023